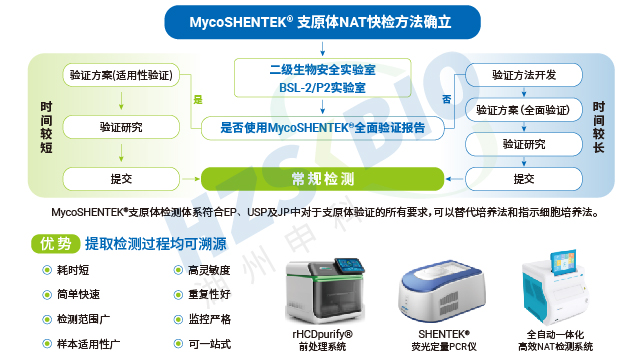
目前支原体检测主要有培养法、指示细胞培养法和核酸扩增技术(NAT)法三类,三者在性能与适用场景上差异明显。培养法作为检测金标准,灵敏度极高,但检测周期长达 28 天,手动操作需数天,依赖较高水平的操作技能,且因使用活菌株作为阳性质控,污染风险高,需在特殊实验室开展,检测前还需进行培养基灵敏度验证。指示细胞培养法为药典认可的传统方法,成本较低,但检测周期仍需 14-20 天,灵敏度偏低,同样存在活菌株污染风险,无法满足快速放行需求。NAT 法(核酸扩增法)检测周期只需 3-7 小时,手动操作时间为数小时,采用灭活菌株降低污染风险,样本需求量少、灵敏度高,但无法区分死菌与活菌,且需要开展充分验证,对操作人员的专业技能有一定要求,已逐步成为生物制药企业产品放行检测的youxia方案。
EP 新规明确支原体验证菌株 GC/CFU 比值<10,需在指数阶段收获以保障活性与分散性。天津细胞疗法产品支原体检测使用性验证
细胞和基因治疗领域正加速发展,国内以 CAR-T、间充质干细胞、AAV 基因治疗等新型生物制品势头正盛。这类产品与传统制药差异明显,给支原体检测带来全新挑战:批产量小但批次多,多数待检测样品含高达 10⁷个活细胞,且基质复杂如高蛋白、全血、高浓度质粒等。更关键的是,新型生物制品终末灭菌难度极大,需从起始材料、原物料到全工艺过程严格控污,而支原体污染隐蔽性强、危害大,成为质量安全控制的主要痛点,也推动着检测方法向更高效、抗干扰的方向升级。
广东重组药物支原体检测快速检测湖州申科已为多家头部企业提供支原体检测方案,支持 BLA/NDA 申报。
湖州申科的支原体培养法样品检测流程严格遵循 USP 标准,步骤规范且逻辑严谨。接种环节:每 100mL 液体培养基接种 10mL 供试品,每类固体培养基接种 0.2mL 供试品;培养条件:置于 36±1℃、5-10% CO₂的湿润环境中培养 28 天。继代培养需在特定时间点开展:接种后第 2-4 天、第 6-8 天、第 13-15 天、第 19-21 天,每次从每种液体培养基中吸取至少 0.2mL,接种至对应固体培养基继续培养不少于 14 天,其中第 20-21 天的继代培养需持续 7 天。观察频率为每 2-3 天一次,若液体培养物出现颜色变化,需立即进行继代培养,再通过与阴阳性对照培养基的对比,完成结果判定,确保检测无遗漏、无偏差。
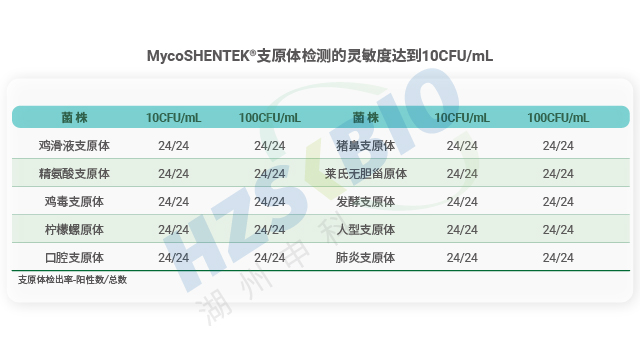
AdvSHENTEK 一体化支原体检测试剂盒具备较广的检测覆盖范围与极强的专属性,能应对各类潜在污染风险。试剂盒可准确检出近 200 种微生物,包括支原体、螺原体、无胆甾原体、虫原体及中间原体,覆盖生物药生产中常见的污染菌株类型。经严格验证,对鸡滑支原体、精氨酸支原体、猪鼻支原体、肺炎支原体等多种菌株,在 10CFU/mL 和 100CFU/mL 浓度下的阳性检出率均达到 24/24,其中包含多个 ATCC 标准菌株。同时,试剂盒专属性强,无交叉干扰现象,能有效区分目标菌株与其他非目标微生物,避免假阳性结果,确保检测数据的准确性,为企业排查支原体污染提供可靠保障。
湖州申科支原体检测验证菌株涵盖 10 余种,满足不同检测场景验证需求。
质控结果是支原体 NAT 检测可靠性的前提,需严格遵循判定标准,且需结合实验室实际条件验证适配的标准阈值。质控样品的判定规则明确:NTC(无模板对照)的 FAM 信号需 2 复孔 Ct≥40 或无明显扩增曲线,VIC 信号需 2 复孔 Ct<35 且呈有效 “S” 型扩增;NCS(阴性对照)判定标准与 NTC 一致;PC(阳性质控)的 FAM 信号需 2 复孔 Ct<35 且呈有效 “S” 型扩增,PCS(阳性对照底物)判定标准与 PC 一致。只有质控结果全部满足要求,才能进一步分析样本结果,若质控不达标,需排查设备、试剂、操作等环节的问题并重新检测。
实验室需分区操作支原体检测,避免阴阳性样本交叉污染,配备单独耗材。江苏细胞疗法产品支原体检测指示细胞培养法
支原体检测试剂盒需覆盖常见污染菌株,避免因菌株遗漏导致漏检。天津细胞疗法产品支原体检测使用性验证
建立可靠的支原体检测 NAT 平台需整合实验室建设、人员培训、污染控制、方法验证四大关键要素,同时依托完善的一站式方案。实验室建设需实现工作区域严格划分与完整配套设备部署,为检测提供硬件支撑。人员需接受规范的现场实验操作培训,熟练掌握检测流程与问题排查技巧。污染控制需贯穿全流程,遵循分区操作、规范消毒、废弃物处理等要求,从源头规避污染风险。方法验证需覆盖检测限、专属性、耐用性等指标,确保方法合规可靠。湖州申科提供的一站式方案包含硬件设备、试剂盒产品与使用方案,同时提供污染防控规范指导、性能验证方案与报告,助力生物制品 QC 部门快速搭建高效、合规的支原体检测平台。
天津细胞疗法产品支原体检测使用性验证