进行RIP-qPCR实验的主要目的:是研究和验证特定蛋白质与RNA分子之间的相互作用。这项技术结合了免疫沉淀(用于捕获蛋白质-RNA复合物)和实时荧光定量PCR(用于定量检测特定RNA分子的表达水平),从而提供了一种有效手段来分析细胞内蛋白质与RNA的结合情况。通过RIP-qPCR实验,研究人员可以识别与特定蛋白质结合的RNA分子,进一步了解这些RNA分子在细胞内的功能、定位以及调控机制。这种相互作用的分析对于深入理解转录后调控、RNA稳定性、剪接变体选择以及非编码RNA的功能等生物学过程至关重要。此外,RIP-qPCR还可用于验证其他实验结果,如基因表达谱、蛋白质组学或生物信息学分析所揭示的潜在蛋白质-RNA相互作用。通过结合多种实验方法,研究人员可以获得更详细的细胞调控网络视图,为疾病机制的研究和新药开发提供有力支持。总之,RIP-qPCR实验的目的在于揭示细胞内蛋白质与RNA的相互作用关系,深化我们对基因表达调控和细胞功能的认识,并为生物医学研究提供有价值的实验依据。若想要快速了解RIP-qPCR实验技术,可以采取哪些方法。广西RNA免疫共沉淀RIP PCR
进行RIP实验时,抗体的选择是实验成功的关键之一。以下是选择抗体时需要考虑的几个要点。1. 特异性:首要考虑的是抗体的特异性。必须选择能够特异性识别并结合目标蛋白的抗体,以避免非特异性结合和背景噪音。可以通过查阅文献、抗体供应商提供的数据或进行预实验来验证抗体的特异性。2. 亲和力:抗体的亲和力也是重要的考虑因素。高亲和力的抗体能够更紧密地结合目标蛋白,提高免疫沉淀的效率。可以选择经过验证的高亲和力抗体,或者通过预实验比较不同抗体的结合能力。3. 物种来源和反应性:根据实验需求选择适当的抗体物种来源和反应性。确保抗体能够与样本中的目标蛋白发生特异性反应,同时避免与其他非目标蛋白发生交叉反应。4. 兼容性:考虑抗体与实验流程的兼容性。某些抗体可能不适用于特定的实验条件或步骤,因此在选择抗体时需要仔细查阅抗体说明书和实验方案。综上所述,进行RIP实验时,应选择具有高特异性、高亲和力、适当物种来源和反应性,以及与实验流程兼容的抗体。通过仔细评估和选择抗体,可以提高实验的准确性和可靠性。安徽RNA免疫共沉淀检测RIP SequenceRIP实验后,如何分析RIP实验结果。

做好RIP-seq实验要点。实验设计:确保有明确的实验目的和假设,并设计适当的对照实验。例如,可以设置阴性对照和阳性对照(使用已知与目标蛋白结合的RNA)来验证实验的有效性和特异性。样本处理:在收集和处理样本时,要防止RNA降解和污染。使用无RNase的试剂和耗材,并在冰上操作以维持低温环境。避免反复冻融样本,因为这可能导致RNA降解。抗体选择:选择高质量、特异性强的抗体进行免疫沉淀。确保抗体能够特异性地识别并结合目标蛋白,以减少非特异性结合和背景噪音。洗涤步骤:在免疫沉淀后,进行充分的洗涤以去除非特异性结合的RNA和蛋白质。RNA提取与质量控制:从免疫沉淀复合物中提取RNA时,要确保使用适当的方法并遵循RNA提取的最佳实践。对提取的RNA进行质量控制,如测定浓度、纯度和完整性,以确保其适用于后续的测序分析。测序与数据分析:选择合适的测序平台和参数进行RIP-seq实验。结果验证:对RIP-seq实验的结果进行验证是很重要的。可以使用其他技术(如RIP-qPCR)来验证特定RNA与目标蛋白的结合情况,以确保结果的准确性和可靠性。
RIP-qPCR实验技术具有多个优点和一些潜在的缺点。优点:特异性高:RIP-qPCR结合了免疫沉淀和qPCR技术,能够特异性地识别并结合目标RNA结合蛋白(RBP)及其结合的RNA,降低非特异性结合的可能性。灵敏度高:qPCR技术具有高灵敏度,能够检测到低丰度的RNA分子,使得RIP-qPCR能够准确测量细胞中RNA与蛋白质的相互作用。定量准确:通过实时监测荧光信号,RIP-qPCR可以对目标RNA进行精确定量,提供可靠的定量数据。应用范围大:RIP-qPCR技术适用于多种生物样本和实验条件,可用于研究不同细胞类型、组织或生物体中的RNA-蛋白质相互作用。缺点:技术复杂性:RIP-qPCR涉及多个步骤,包括细胞裂解、免疫沉淀、RNA提取、逆转录和qPCR等,操作相对复杂,需要经验丰富的实验人员。抗体依赖性:实验结果的准确性和特异性高度依赖于所使用的抗体的质量和特异性。非特异性抗体可能导致假阳性或假阴性结果。RNA易降解:RNA分子在操作过程中容易降解,特别是在不适当的实验条件下,如存在RNase污染或操作时间过长。综上所述,RIP-qPCR实验技术具有高特异性和灵敏度,能够准确测量RNA与蛋白质的相互作用,但操作复杂、抗体依赖性强、RNA易降解以及成本较高是其潜在的缺点。RIP-qPCR实验技术是一种强大的研究RNA与蛋白质相互作用的方法,也存在一些不足之处。
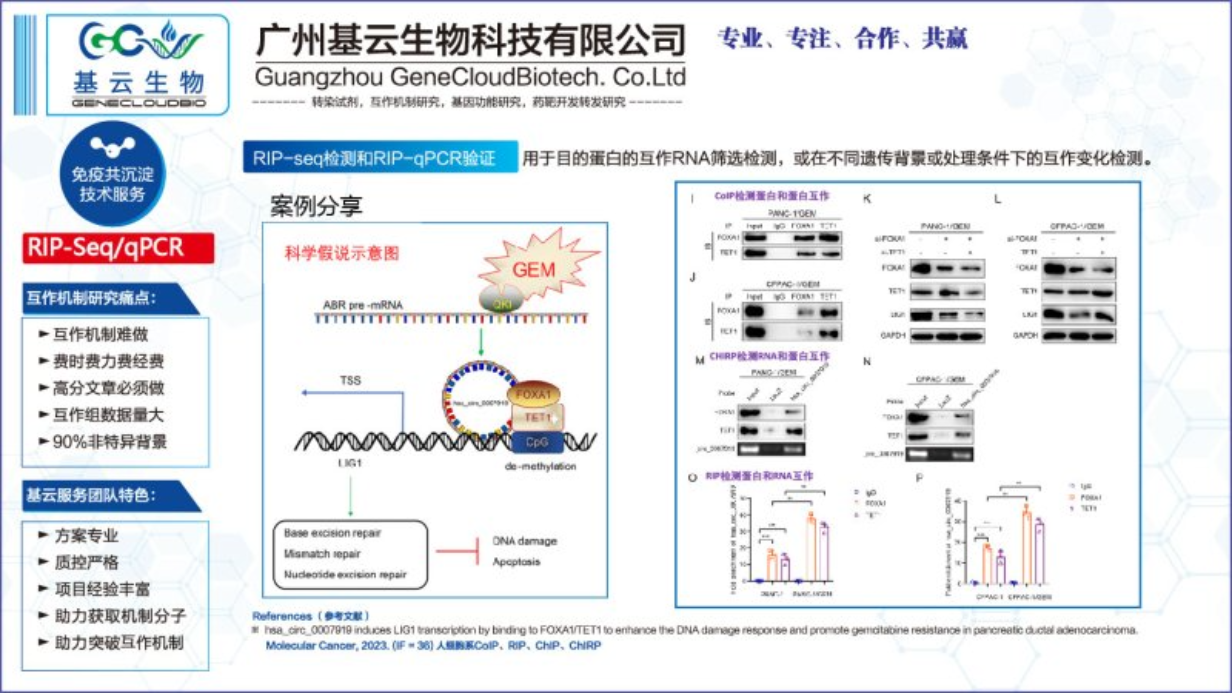
RIP-qPCR实验技术的原理是基于RNA免疫沉淀(RNA Immunoprecipitation, RIP)与实时荧光定量PCR(quantitative real-time PCR, qPCR)的结合。首先,通过RIP技术,利用抗体特异性地识别并结合目标RNA结合蛋白(RBP),将RBP与其结合的RNA一起沉淀下来。这一步骤依赖于抗体与RBP之间的特异性相互作用,确保只有与目标RBP结合的RNA被沉淀。接下来,从沉淀的复合物中提取RNA,并通过逆转录将其转化为cDNA。然后,利用qPCR技术对特定的RNA分子进行定量检测。在qPCR反应中,通过荧光信号的实时监测,可以准确测量PCR产物的累积量,从而实现对目标RNA的定量分析。综上所述,RIP-qPCR实验技术的原理是通过特异性抗体沉淀目标RBP及其结合的RNA,然后利用qPCR对沉淀下来的RNA进行定量检测。这项技术结合了RIP的特异性和qPCR的灵敏性,为研究细胞内RNA与蛋白质的相互作用提供了有力工具。通过这种方法,可以深入了解RNA与蛋白质在细胞内的结合情况,揭示转录后调控网络的动态过程。RIP实验的具体实验步骤是什么。湖北RNA蛋白相互作用RIP qPCR
RIP技术用抗体沉淀RNA-蛋白复合物,经纯化后进行qPCR验证或测序,是研究细胞内RNA与蛋白结合的关键工具。广西RNA免疫共沉淀RIP PCR
进行RIP-qPCR实验,应该注意以下几个关键问题,以确保实验的成功和准确性。1. 样本处理:确保样本新鲜且未受污染,避免RNA降解。在处理过程中使用无RNase的试剂和耗材,并在冰上操作以维持低温环境。2. 抗体选择:选择特异性强的抗体进行免疫沉淀,这是实验成功的关键。验证抗体的特异性和效力,以确保准确捕捉目标RNA-蛋白质复合物。3. 引物设计:设计特异性针对目标RNA的引物,避免非特异性扩增。确保引物的质量和纯度,以获得可靠的qPCR结果。4. 实验对照:设置适当的对照实验,如使用非特异性抗体作为阴性对照,以验证实验结果的特异性和准确性。5. 操作规范:严格遵守RNA操作规范,避免RNA酶的污染。确保实验环境的清洁和无菌,以减少误差和干扰。6. 数据分析:使用适当的统计方法和软件分析实验数据,确保结果的准确性和可靠性。注意识别并排除异常值,以获得真实可信的结果。综上所述,进行RIP-qPCR实验时,你应注意样本处理、抗体选择、引物设计、实验对照、操作规范和数据分析等关键问题。通过仔细考虑和遵循这些注意事项,可以提高实验的成功率和准确性。广西RNA免疫共沉淀RIP PCR