肺纤维化(英语:Pulmonaryfibrosis)是一种肺随时间瘢痕化的疾病。症状包括呼吸困难、干咳、疲倦、体重下降和杵状指。可能的并发症有肺动脉高压、呼吸衰竭、气胸和肺*。肺纤维化的病因涵盖环境污染、特定药物、结缔组织疾病、***(包括COVID-19和相关的SARS病毒)及间质性肺病。最常见的是特发性肺纤维化(IPF),这是一种原因不明的间质性肺病。通常基于症状、医学影像、肺活检和肺功能测试作出诊断。肺纤维化目前尚无***可能,可用的***手段也有限。***旨在改善症状,可能包括氧疗和肺康复。一些药物可用于尝试延缓***的进展。有时可考虑进行肺移植。全球至少有500万人罹患本病。预期寿命一般不超过五年。通过肺纤维化模型,科学家可以研究不同药物对疾病进程的影响。河北专业的肺纤维化模型实验外包
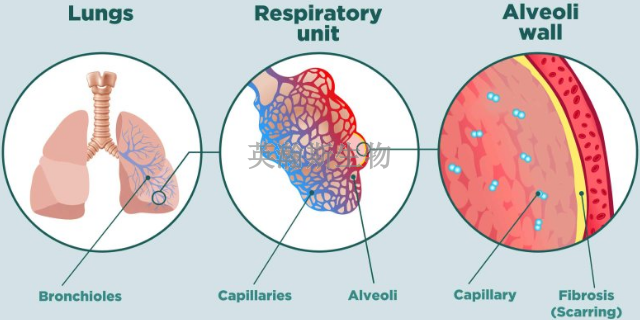
在肺纤维化模型中,一个明显且关键的变化就是肺泡壁的逐渐增厚。这个过程是由于持续的炎症、细胞损伤和修复机制的异常活跃所导致的。随着炎症的持续存在,免疫细胞会不断释放炎症介质,这些介质会刺激肺泡壁中的细胞增殖,并导致胶原蛋白和其他纤维组织的过量沉积。随着时间的推移,这些沉积物不断积累,使得肺泡壁变得坚硬而厚实,从而限制了肺泡的扩张和收缩能力。这种增厚不仅影响了气体的交换效率,还使得肺部难以有效地进行氧气和二氧化碳的交换,比较终导致肺功能的明显下降。这一过程在肺纤维化模型中得到了精细的模拟,为研究疾病的进程和疗愈提供了重要的参考。河北专业的肺纤维化模型实验外包肺纤维化模型有助于评估不同药物在肺纤维化疗愈中的安全性。
肺纤维化模型发展时间:给药后第 7 天肺组织大多呈重度肺泡炎改变,肺泡腔及肺间质内有大量中性粒细胞浸润,部分肺泡腔破坏或消失,肺间隔内成纤维细胞和***增生,与正常肺组织对比差别明显;给药后第14天,肺纤维化开始形成。巨噬细胞、中性粒细胞等炎性细胞明显减少,成纤维细胞增多,肺泡间隔明显增厚,有胶原沉积。给药后第28天,多数小鼠发生弥漫性肺间质纤维化,肺间质被胶原纤维和成纤维细胞替代,肺泡壁破坏,肺大泡形成,但仍可见炎性细胞浸润。
肺纤维化是一种肺部疾病,发生于受损和出现***的肺组织。这种增厚、僵硬的组织使肺更加难以正常运作。随着肺纤维化的恶化,您会逐渐感觉气短。与肺纤维化相关的瘢痕形成可由多种因素引起。但在大多数情况下,医生无法查明问题的根源。如果无法发现原因,就称为特发性肺纤维化。肺纤维化引起的肺损伤无法修复,但药物和疗愈有时可帮助缓解症状和提高生活质量。英瀚斯生物,专业成熟的动物肺纤维化模型构建方法,适用于大鼠、小鼠。已有成功案例。科学家通过肺纤维化模型发现了一些新的疾病疗愈靶点。
肺纤维化模型在模拟肺纤维化的病理过程中,深入揭示了氧化应激在疾病进程中的关键作用。氧化应激是指机体内氧化与抗氧化作用失衡,导致活性氧自由基及其相关产物过量积累,进而对细胞和组织造成损伤的一种状态。在肺纤维化模型中,研究人员发现氧化应激与肺纤维化的发生和发展密切相关。当肺部受到损伤时,氧化应激反应被激发,产生大量的活性氧自由基,这些自由基会攻击肺部细胞和组织,导致细胞损伤和死亡,进而促进肺纤维化的形成。因此,肺纤维化模型不仅为我们揭示了氧化应激在肺纤维化中的作用机制,也为开发针对氧化应激的疗愈策略提供了重要的实验依据。研究人员通过肺纤维化模型发现了一些新的疾病标志物。甘肃小鼠肺纤维化模型
肺纤维化模型的选择需要评估合适的模型来重现正在研究的纤维化形式。河北专业的肺纤维化模型实验外包
在肺纤维化模型中,肺组织经历了一个复杂而微妙的转变过程,即从炎症逐渐过渡到纤维化。这个过程模拟了人类肺部在遭受长期炎症损伤后,如何逐渐失去其原有的弹性和功能,转而形成坚硬的纤维组织。炎症阶段,肺组织中的免疫细胞被激发,释放出各种炎症介质,导致肺组织受损。随着时间的推移,这些炎症损伤无法得到有效修复,肺组织开始尝试通过纤维化来自我修复,然而这一过程却导致了肺组织的进一步硬化和功能障碍。肺纤维化模型不仅为我们揭示了这一转变的详细过程,也为深入研究肺纤维化的发病机制和治疗方法提供了重要依据。河北专业的肺纤维化模型实验外包