双光子显微镜的基本原理是:在高光子密度的情况下,荧光分子可以同时吸收2个长波长的光子,在经过一个很短的所谓激发态寿命的时间后,发射出一个波长较短的光子;其效果和使用一个波长为长波长一半的光子去激发荧光分子是相同的。双光子激发需要很高的光子密度,为了不损伤细胞,双光子显微镜使用高能量锁模脉冲激光器。这种激光器发出的激光具有很高的峰值能量和很低的平均能量,其脉冲宽度只有100飞秒,而其周期可以达到80至100兆赫兹。在使用高数值孔径的物镜将脉冲激光的光子聚焦时,物镜的焦点处的光子密度是比较高的,双光子激发只发生在物镜的焦点上,所以双光子显微镜不需要共聚焦,提高了荧光检测效率。双光子显微镜比单光子共聚焦显微镜较大的不同在于无须使用孔限制光学散射。美国investigator双光子显微镜扫描深度

通过对微型光学系统的重新设计,FHIRM-TPM2.0成像视野扩大至420×420平方微米,微型物镜的工作距离扩展至1毫米,以实现非侵入式成像;嵌入了可拆卸的快速轴向扫描模块,实现了180微米深度的三维体成像和多平面快速切换的实时成像。该模块由一个快速的电动变焦透镜和一对中继透镜组成,在不同深度成像时保持放大倍率恒定。其中,变焦模块重量1.8克,研究人员可根据实验需求自由拆卸。此外,新版微型化成像探头还可整体即时拔插,极大地简化了实验操作,避免了长周期实验时对动物的干扰。在重复装卸探头追踪同一批神经元时,视场旋转角小于0.07弧度,边界偏差小于35微米。国内双光子显微镜原理这种双光子显微镜的视场是普通显微镜的10倍。

临研所、病理科和科研处邀请北京大学王爱民副教授在2020年12月22日做了题目为“新一代微型双光子显微成像系统介绍及其在临床医疗诊断”的学术报告。学术报告由临研所医学实验研究平台潘琳老师主持。王爱民,北京大学信息科学技术学院副教授,毕业于北京大学物理系,获学士、硕士学位,后于英国巴斯大学物理系获博士学位。该研究组研发的微型双光子显微镜,第1次在国际上获得了小鼠大脑神经元和神经突触清晰稳定的动态信号,该成果获得了2017年度“中国光学进展”和“中国科学进展”,并被NatureMethods评为2018年度“年度方法--无限制行为动物成像”。目前,该研究组正在研究新一代双光子显微成像技术在临床诊断中的应用,为未来即时病理、离体组织检测、术中诊断等提供新的影像手段和分析方法。
双光子显微成像技术不是什么新技术,早在20多年前就有了,目前已经在生命科学和材料科学中广泛应用。几年前双光子过期后,已经推出自己的双光子显微镜的厂家估计不少于10家以上。即便如此,世界上很多实验室都搭双光子,自己搭的好处有很多,首先是便宜,尤其是实验室已经有飞秒激光器,那就更很省钱了。其次是灵活,可以选择针对特殊用途的搭配,改动也灵活。好处就是可以锻炼队伍,一趟走下来可以把新手带出来,后期维护也更加自由。当然坏处也不少,首先是操心,特别是第1次搭的时候,开始要想方案,后来要解决各种实际问题。其次是花时间,加上买配件的时间,比买一台现成的商业化双光子耗时长。现在已经有不少关于如何搭双光子显微镜的文章,各种protocol,大多是老外写的,中文的较少。其实完全自己搭一套好用的系统还是不容易的,尤其是没有经验的时候,容易走弯路,多花钱,也多花时间,再加上双光子的重要器件都需要从国外购买,在国内买这些东西耗时较长。因此,我想总结一下我们的经验,贴出来分享,希望能帮到想自己动手的实验室,双光子显微镜使用的是可见光或近红外光作为光源。
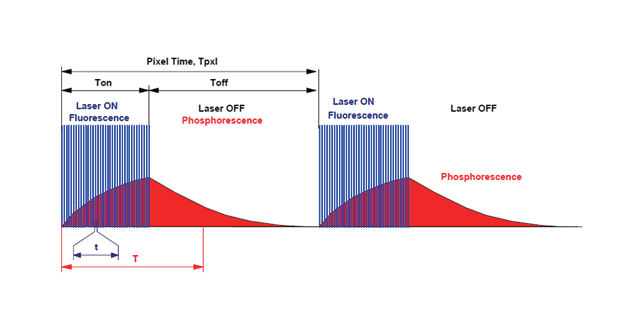
从双光子的原理和特点我们就可以明显的得出双光子的优点:☆光损伤小:由于双光子显微镜使用的是可见光或近红外光作为激发光源,这一波段的光对细胞和组织的光损伤小,适用于长时间的研究;☆穿透能力强:相对于紫外光,可见光和近红外光都具有更强的穿透能力,因而受生物组织散射的影响更小,解决对生物组织中深层物质的层析成像研究问题;☆高分辨率:由于双光子吸收截面很小,只有在焦平面很小的区域内可以激发出荧光,双光子吸收局限于焦点处的体积约为波长3次方的范围内;☆漂白区域小:由于激发只存在于交点处,所以焦点以外的区域都不会发生光漂白现象;☆荧光收集率高:与共聚焦成像相比,双光子成像不需要光学滤波器(共焦),这样就提高了对荧光的收集率,而收集率的提高直接导致图像对比度的提高;☆图像对比度高:由于荧光波长小于入射波长,因而瑞利散射产生的背景噪声只有单光子激发时的1/16,降低了散射的干扰;☆光子跃迁具有很强的选择激发性,所以可以对生物组织中一些特殊物质进行成像的研究;双光子显微镜工作原理是利用两个光子的能量相加达到荧光激发能量阈值,来激发样品中荧光分子发出荧光信号。国外激光荧光双光子显微镜授权商
双光子显微镜有哪些应用呢?美国investigator双光子显微镜扫描深度
共聚焦显微可以呈现这么漂亮的图像,是不是什么样品都可以用共聚焦显微镜拍拍拍.....得到各种各样清晰漂亮的图像呢?答案是否定的,任何事物都有优缺点,何况一台仪器呢,共聚焦显微镜也是有自己的局限,共聚焦有哪些局限呢:1.共聚焦显微镜只能拍摄约200um以内的的样品,对于厚的或者样品不能进拍摄;2.共聚焦显微镜由于是逐点进行扫描,对样品的光毒性还是比较大的,特别是拍摄活细胞样品时就更容易对样品进行淬灭;3.由于光照射的区域几乎能通过这个Z轴的层面,所以对于空间定点光刺激的实验定点位置就不是特别精确;并且激光共聚焦显微镜没有纯紫外进行激发,对于一些特殊激发波长的实验,效率非常低。双光子显微镜的基本原理是:在高光子密度的情况下,荧光分子可以同时吸收2个长波长的光子,在经过一个很短的所谓激发态寿命的时间后,发射出一个波长较短的光子;其效果和使用一个波长为长波长一半的光子去激发荧光分子是相同的。双光子激发需要很高的光子密度,为了不损伤细胞,双光子显微镜使用高能量锁模脉冲激光器。这种激光器发出的激光具有很高的峰值能量和很低的平均能量,其脉冲宽度只有100飞秒,而其周期可以达到80至100兆赫兹。美国investigator双光子显微镜扫描深度