- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
2018版《指导要求》说明外泌体没有限定单一的分离手段,多种手段都可以进行细胞外囊泡的富集。《指导要求》编写者们认为“高回收率,低特异性”的富集手段是指那些富集囊泡的同时会有大量的非囊泡组分被富集,甚至细胞的整个分泌组都会被掺入其中,归入这一类的分离手段主要包括通过改变电荷或通过高聚物作用的沉淀试剂盒、低分子量截流的超滤分离、超长时间和超高离心力的超速离心等。Wako的MagCapture™ExosomeIsolationKitPS(产品编号299-77603(2tests),293-77601(10tests)),使用PS亲和法对外泌体进行提取,损失小且能获得高纯度的外泌体。超离法是较常用的外泌体纯化手段,采用低速离心、高速离心交替进行,可分离到大小相近的囊泡颗粒。上海外泌体提取试剂服务电话
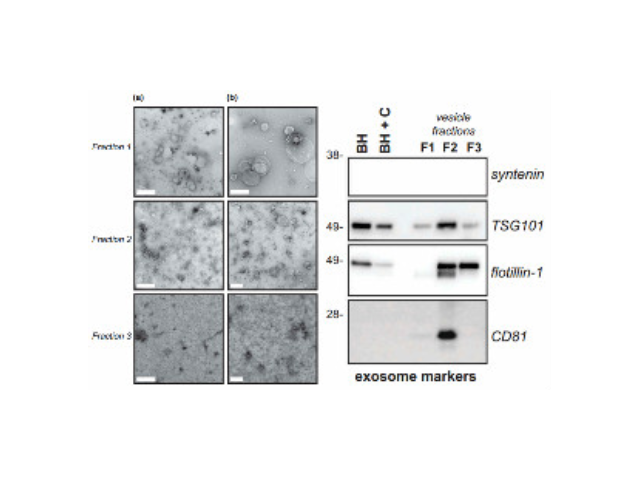
外泌体提取:1、过滤。超滤膜也可用于分离外泌体。根据外泌体的大小,从蛋白质和其他大分子中分离外泌体。较常见的过滤膜具有0.8μm、0.45μm或0.22μm的孔径,可用于收集大于800nm、400nm或200nm的外泌体,也有设计成微柱多孔硅纤毛结构以分离40-100nm外泌体:不过,该方法由于过滤膜的粘附,可能会损失外泌体,并且过滤时的压力和剪切力,可能会使外泌体变形受损。2、基于聚合物的沉淀技术。基于聚合物的沉淀技术通常包括将样本与含聚合物的沉淀溶液混合,在4℃温育并低速离心。用于聚合物沉淀的较常见聚合物之一是聚乙二醇(PEG)。用这种聚合物沉淀具有许多优点,包括对分离的外泌体影响小、pH中性等。目前大多数快速分离外泌体的商品化试剂盒都是基于此方法。然而基于聚合物的沉淀方法可能会同时分离非囊泡污染物(包括脂蛋白)而且,聚合物材料的混杂可能会影响下游分析杭州外泌体提取试剂厂家批发价由于国内有关外泌体提取试剂的缺乏,我国对外泌体的研究还基本依赖于过程繁琐的超速离心和进口提取试剂盒。

外泌体与神经退行性疾病:外泌体可能促进或限制大脑中未折叠和异常折叠的蛋白质的聚集。AD病人脑脊液外泌体中均可检测到Tau和Aβ蛋白。类似的现象也在PD和ALS疾病中发现。PD病人脑脊液外泌体可检测到α-synuclein,ALS病人外泌体中也可以检测到SOD1或TDP-43。外泌体与疾病诊断(应用潜能):外泌体生成机制表明,通过分析外泌体的组分,可以帮助识别其来源的细胞类型。这一特性已被应用于开发心血管疾病,神经系统疾病和一些病症的分子诊断方法,也在肝肾肺相关疾病中进行研发测试。将沉淀物用PBS缓冲液进行悬浮,使外泌体悬浮于液体上层。
外泌体的提取方法:1.超速离心法(差速离心)。超离法是较常用的外泌体纯化手段,采用低速离心、高速离心交替进行,可分离到大小相近的囊泡颗粒。超离法因操作简单,获得的囊泡数量较多而广受欢迎,但过程比较费时,且回收率不稳定(可能与转子类型有关),纯度也受到质疑;此外,重复离心操作还有可能对囊泡造成损害,从而降低其质量。2.密度梯度离心。在超速离心力作用下,使蔗糖溶液形成从低到高连续分布的密度阶层,是一种区带分离法。通过密度梯度离心,样品中的外泌体将在1.13-1.19g/ml的密度范围富集。此法获得的外泌体纯度较高,但步骤繁琐,耗时,对离心时间极为敏感逐渐取代超速离心法并推广开来。有些试剂盒操作简便,不用超速离心。

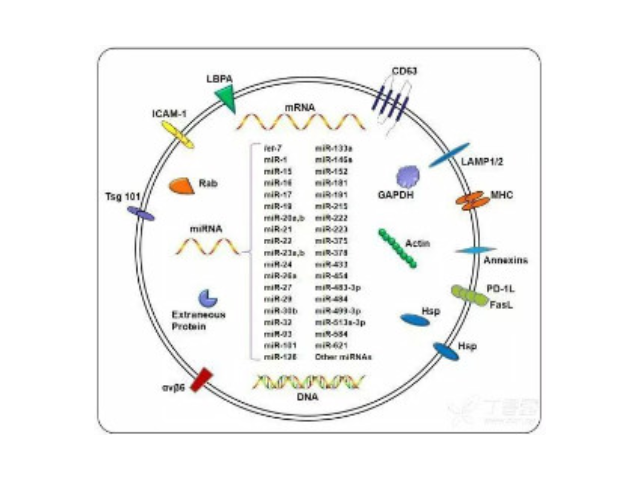
由于外泌体的特殊结构和功能,使得它具有潜在的应用价值,一方面可以作为诊断多种疾病的生物指标,另一方面也可以作为治病手段,未来有可能作为药物的天然载体用于临床治病。外泌体的分离纯化一直是科研工作者关注的问题,获得高纯度的外泌体对后续的研究至关重要。据了解,目前人们多采用超速离心、免疫磁珠、超滤、沉淀或试剂盒等方法实现外泌体的提取分离。外泌体携带大量特异性的蛋白质(如细胞因子、生长因子)以及功能性的mRNAs、miRNAs等生物活性物质,在体内参与细胞通讯、细胞迁移、促血管新生和抗一些病症免疫等生理过程,与多种疾病的发生和进程密切相关。磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点。济南外泌体提取试剂厂家供应
这些试剂盒不需要特殊设备,随着产品不断更新换代,提取效率和纯化效果逐渐提高。上海外泌体提取试剂服务电话
CD47是信号调节蛋白α(SIRPα,也称为CD172a)的配体,CD47-SIRPα间的结合能够发出“不要吃我”的信号,从而压制吞噬作用。病基因RAS能够促进胰腺病细胞增殖,增强胞饮作用从而促进一些病症细胞摄取外泌体。合成纳米颗粒对细胞有一定毒性作用,但使用外泌体能够较小化对细胞的毒性。研究人员发现,CD47和病基因KRAS驱动的胞饮作用都会压制外泌体被循环系统的清理,并增强胰腺病细胞对外泌体的特异性。所以,外泌体的这种特性增强了它们通过递送RNAi来特异性靶向胰腺病中的KRAS的能力,并且使用外泌体作为单一靶向剂显着改善了所有实验PDAC小鼠模型的总生存期。上海外泌体提取试剂服务电话
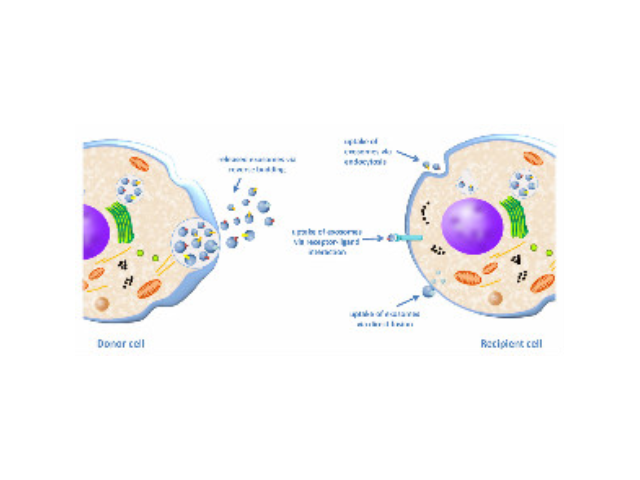
1996年GRaposo等发现类似于B淋巴细胞的免疫细胞也会分泌抗原呈递外泌体(antigenpresentingvesicle),所分泌的外泌体可以直接刺激效应CD4+细胞的抗一些病症反应。2007年HValadi等进一步发现细胞之间可以通过外泌体中RNA交换遗传物质。随着有关外泌体研究越来越多,研究者发现它普遍参与了机体免疫应答、抗原呈递、细胞分化、一些病症生长于侵袭等各种生物过程中。目前的主流观点认为,外泌体的产生过程为:细胞膜内陷,形成内体(endosome),再形成多泡体(multivesicularbodies,MVB),较后分泌到胞外成为外泌体。外泌体中携带有母细胞的多种蛋白质、...
- 无锡外泌体提取试剂生产厂家 2026-05-28
- 太原外泌体提取试剂平均价格 2026-05-28
- 杭州外泌体提取试剂直销厂家 2026-05-11
- 郑州外泌体提取试剂产品介绍 2026-05-06
- 上海外泌体提取试剂报价 2026-04-30
- 昆明正规外泌体提取试剂 2026-04-29
- 杭州外泌体提取试剂服务电话 2026-04-27
- 宁波外泌体提取试剂哪里买 2026-04-17
- 重庆正规外泌体提取试剂生产厂家 2026-04-16
- 无锡正规外泌体提取试剂生产厂家 2026-04-12
- 石家庄外泌体提取试剂直销厂家 2026-04-02
- 正规外泌体提取试剂平均价格 2026-03-25
- 济南正规外泌体提取试剂厂家现货 2026-03-25
- 石家庄正规外泌体提取试剂报价 2026-03-23
- 金华外泌体提取试剂厂家 2026-03-22
- 北京外泌体提取试剂直销价 2026-03-19


- 长沙正规细胞外基质胶供应商 06-08
- 芜湖正规无血清细胞冻存液哪里买 06-07
- 杭州正规原代细胞分离试剂盒产品介绍 06-07
- 北京正规细胞高效转染试剂直销价 06-06
- 南昌外泌体提取试剂 06-06
- 浙江糖原染色试剂盒进货价 06-05
- 杭州正规无血清细胞冻存液哪家好 06-05
- 上海无血清细胞冻存液厂家批发价 06-04
- 济南无血清细胞冻存液生产厂家 06-04
- 江西正规糖原染色试剂盒直销价 06-03